新闻 | 拯救伤员生命的合成血液和血液制品
2022-08-22
合成生物学是一种制造与生物系统相互作用的装置、药物和其他技术的新方法。与利用对病理学、生理学和经验观察的理解来影响生物系统的传统医学创新方法不同,合成生物学利用了近几十年来生物技术的进步,没有依赖天然化合物与人类生物系统的相互作用来获得治疗益处,而是通过对人类生物学的更好理解,结合现代人工制造的工具,实现了更可靠、可扩展和可定制化的创新治疗。表1显示了几种方法和具体示例。对合成生物学的兴趣远远超出了医学领域,2021年的投资估计为114亿美元。美国国防高级研究计划局的“生物铸造(live Foundries)”计划“旨在实现适应性、可扩展和按需生产……关键的高价值分子,这些分子通常极其昂贵,无法在国内获得,或无法使用传统方法制造。”应用包括工业化学品、药品、涂料和粘合剂;转基因作物和微生物生产生物燃料;甚至将生物成分整合到服装和建筑材料中,以增强耐用性和保护性能。类似技术的医疗应用经常可以找到。
合成血液定义和应用
从现代医学诞生开始,“合成血液”的概念就迅速吸引了医生和研究人员。在哈维于1616年描述了血液循环之后不久,克里斯托弗·雷恩爵士在1656年写下了他的各种物质注入实验:
“我通过静脉向一条活狗的血液中注入了大量的葡萄酒和麦芽酒,直到我让它喝得烂醉如泥,但不久后它就把酒喝光了……”1659年,甚至在寻找血液替代品的过程中,动物间的输血也随之而来。1878年,托马斯注意到乳糜和牛奶之间的化学相似性,将牛奶注入三个病人体内——大部分没有成功。后来一种传统的基于生物学技术维持循环血量或其成分的方法问世,该方法基于来自献血者的血液或基于简单的生理学理解制备的晶体和胶体溶液,然而这种方法持续了几个世纪。在20世纪30年代,由于肾毒性,使用溶解红细胞血红蛋白的有限尝试失败了。在20世纪80年代,对丙型肝炎和人类免疫缺陷病毒(HIV)在捐献血液中传播的担忧,促进了第一次尝试开发来自捐献者的血液成分的人工替代品。此时开始的一些方法的进一步发展今天仍有希望。在考虑“合成血液”的概念时,重要的是要理解这一概念是指应用各种各样的技术方法,以替代或增强患者天然血液的功能。此外,重要的是要理解,虽然血液是一个复杂的器官,确实应该被视为与包含它的血管环境不可分割,但许多“合成血液”的方法只关注血液的一种功能:最常见的是氧气输送,但最近也关注血小板功能。对“合成血液”的综合考虑可能还包括大量用作血浆扩容剂的静脉注射液和血液衍生物,如晶体、胶体如明胶或羟乙基淀粉,以及各种白蛋白产品。此外,还可能包括对标准血浆产品的重要操作,以延长保质期或可及性,如冻干或喷雾干燥。然而,这篇简短的综述将集中在生产血液细胞成分替代品的尝试上,特别是红细胞和血小板。大多数看到“合成血液”一词的医生会把它等同于治疗出血或贫血的产品。值得注意的是,一些人做出了不同的假设,将合成血液视为人类健康表现改善的一种机制。2018年,当一名中国科学家使用CRISPR技术对三个人类胚胎进行基因编辑时,合成生物学在世界范围内引起了广泛关注,据报道,其目的是降低这些胚胎对艾滋病毒感染的敏感性,但这导致了广泛的不安,并对相关科学家进行了伦理审查。假设合成的“超级血液”可以显著提高个人的身体速度、力量和耐力。反过来,这可以让人们在极端条件下工作,或者更轻松地完成日常任务。”职业运动员使用促红细胞生成素和其他血液兴奋剂方法的显著例子将这种想法从科幻领域转移到现实。也许,令人放心的是,意见调查发现“大多数美国人似乎对以这种方式使用合成血液替代品的想法持怀疑态度。”然而,临床医生、研究人员、资助者和伦理审查小组在解释诸如“大多数人(63%)不希望自己体内有合成血液”之类的回答时,当然必须考虑到当时问题的提出背景,如果替代方案是死于失血性出血,想必答复可能会有所不同。
改进当前输血实践的理由
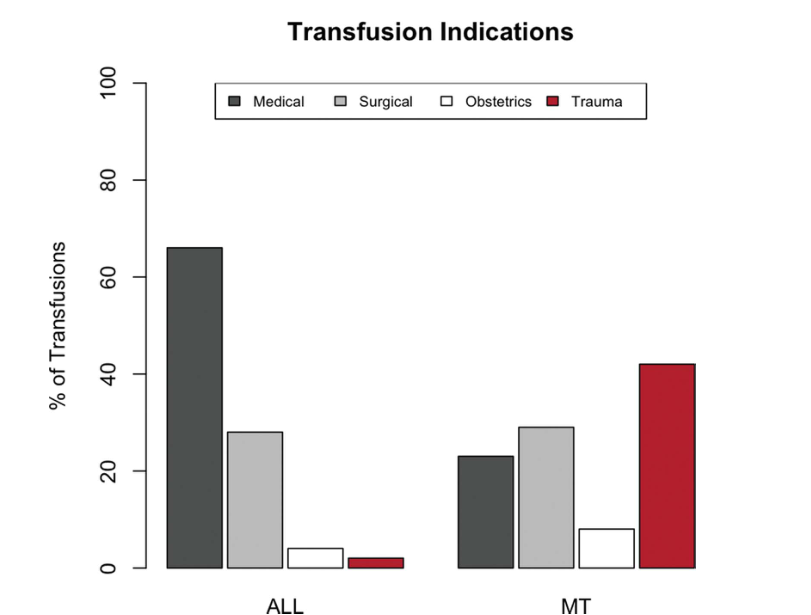
目前的输血实践无疑挽救了全球数百万患者的生命。仅在美国,每年就有近2100万例血液成分输血,全球每年收集的献血量近1.2亿单位。在地方医学中,最常见的输血指征(34%)是恶性肿瘤或其治疗的并发症,其次是贫血的其他医学原因(19%)和手术(18%)。虽然急性创伤仅占总适应症的2%,但创伤是迄今为止大量输血最常见的适应症(图1)。
输血风险过敏反应、因错误输注ABO血型不合血液而导致的急性溶血性输血反应、迟发性溶血性输血反应、发热性非溶血性输血反应、输血相关急性肺损伤和输血相关移植与宿主排斥扥。然而,危及生命的反应非常罕见,登记数据显示输血的发生率仅为60万分之一至230万分之一,在大多数发达国家,通过血液传播传染病筛查的志愿献血者的血液供应现在十分安全, 到2001年,美国艾滋病毒和丙型肝炎传播的风险不到1/100万单位。相比之下,在56个国家,超过50%的血液供应仍然依赖于家庭/替代和有偿献血者。低收入国家只有80%的输血遵循基本质量程序进行传染病筛查。在这些国家,捐献血液中艾滋病毒的流行率估计为0.7%、乙型肝炎2.81% 和丙型肝炎1.00% 。在发展中国家,以可负担的方式替代捐献的血液将获得更大的好处,例如,在尼日利亚,输血是艾滋病毒传播的第二大常见原因。
血液衰竭
严重出血最常见的原因是腹主动脉或髂血管动脉瘤破裂、消化性溃疡疾病、术中出血、围产期出血或外伤。美国每年有超过60,000人死亡,全球有近2,000,000人因出血死亡。这些死亡是由延迟性出血、活动性出血期间延迟救治以及失血性休克的延迟识别引起的。所有这些因素都可能导致所谓的低体温、酸中毒和凝血病的致命三联征。当合并严重的组织损伤时,由此导致的创伤引起的凝血病与近50%的死亡率相关。
快速、严重的出血导致氧气输送不足和大量氧债(oxygen debt)的积累。这种全身性氧债和致命三联体的相关生理紊乱被称为血液衰竭。复苏的主要目标之一,除了最大化减少或停止正在进行的出血,是逆转氧缺乏和偿还累积的氧债。这是通过许多互补的努力来实现的,包括确保足够的全身灌注,恢复足够的血管内容量和携氧能力,补充衰竭水平的凝血因子和血小板。这种方法被称为损伤控制复苏。血液衰竭的管理,一旦建立,甚至预防轻中度患者的失血,都可以考虑使用合成血液和血液制品。以下部分详细介绍了从成熟到未来的各种可能性,这些可能性可能成为复苏医疗设备的一部分,适用于从资源丰富的城市创伤中心到严峻的战场环境等各种环境。
合成红细胞
基于血红蛋白的氧载体(HBOCs)是使用人、牛、猪和海洋蠕虫血红蛋白生产的。天然血红蛋白已经通过聚合、聚乙二醇化和各种其他化学改变进行了修饰,试图降低由与游离血红蛋白相关的一氧化氮清除引起的肾毒性和急性高血压。三种聚合血红蛋白已进入高级开发阶段:HemAssist(巴克斯特公司)、PolyHeme(诺斯菲尔德实验室)和Hemopure(或HBOC-201)。HemAssist是diaspirin交联的人类血红蛋白,最初由莱特曼陆军研究所于20世纪80年代开发,但随后被授权给巴克斯特公司。尽管临床前研究令人鼓舞,心脏手术患者的一项临床试验也是如此,但三项试验因安全问题而提前终止。PolyHeme在一项具有历史对照的人体研究中显示出最初的希望,但随后760名患者的院前和院内使用的三期试验结果因伦理原因而受到批评,据报道未能显示出益处(尽管仍未公布),该产品的生产随后停止。
迄今为止,只有Hemopure(牛血红蛋白的四聚体制剂)在人类中有重要的临床应用。在进行了几项令人鼓舞的小型临床研究后,在骨科手术患者中进行了一项大规模(n = 688名患者)血液透析与红细胞的比较试验,发现血液透析避免了近60%患者的红细胞输注需求,但与更高的不良事件发生率相关,最有可能与血液透析的血管活性有关。聚乙二醇修饰(PEGylated)血红蛋白是另一种减少血管活性效应和游离血红蛋白肾脏沉积的方法。已经开发了几种聚乙二醇化血红蛋白,包括在动物模型中有效但在随机试验中与不良反应相关的Hemospan,导致其生产停止。Sanguinate(新泽西州)被认为是对HBOC-201的理论改进,使用一氧化碳来避免清除一氧化氮。临床应用仅限于蛛网膜下腔出血和镰状细胞危象的病例系列,虽然没有比较试验,但早期结果令人鼓舞。另一种较新的方法是将酪氨酸残基基因工程改造到血红蛋白分子中,使其在聚乙二醇化前保持铁的形式,循环时间令人鼓舞,在小鼠中没有明显的副作用。合成纳米粒子代表了一类新兴的红细胞替代品。有几种潜在的生物相容性纳米粒子壳制剂可以包裹血红蛋白,减少组织外渗和一氧化氮清除。这一领域的著名代表是美国公司kalytore(马里兰州巴尔的摩)正在开发的产品。该产品使用人类血红蛋白和添加的还原剂来减少高铁血红蛋白的形成。制造商是一家大学公司,产品仍处于早期开发阶段,没有注册临床试验。全氟化碳被认为是一种有吸引力的红细胞替代品,因为它们对呼吸气体具有显著的溶解能力。不幸的是,全氟辛烷磺酸不溶于水,乳化全氟辛烷磺酸所需的表面活性剂导致了多种毒性,如流感样综合征、补体激活和血小板减少症,导致产品失效。1989年,美国食品和药物管理局批准氟索尔-达(美国加州洛杉矶阿尔法治疗公司)(一种白蛋白占20%的全氟化碳乳剂)使用。没有一种PFC乳剂被成功开发到临床应用的阶段。“血液制药”是红细胞替代的最新合成生物学方法。一般的方法是用干细胞或红细胞祖细胞接种生物反应器,扩大细胞群,同时将细胞推向红细胞分化途径。产生的细胞是有核红细胞或网织红细胞,取决于包括反应器设计在内的各种因素。美国国防部和其他部门在这一领域投入了大量资金,成功地建立了概念验证系统。然而,迄今为止,用这些方法生产红细胞的成本高得令人望而却步,主要的成本因素是分化和生长因素以及培养基。另一个主要的成本因素是从骨髓或脐带中获取干细胞。iPS细胞技术可能会增加干细胞的可用性,但代表了一系列不同的挑战和成本。使用CRISPR或其他技术对干细胞进行基因操作,可能会产生证明体外生产成本合理的红细胞产品——例如,普遍兼容的红细胞——但这些努力仍处于早期开发阶段。
合成红细胞在非出血性疾病中的应用
有必要简要提及合成红细胞的其他应用。几种疾病状态,包括缺血性心脏病和蛛网膜下腔出血后脑血管痉挛引起的大脑皮质缺血,是由氧气需求和输送之间的不平衡引起的。当血细胞比容过高时,红细胞的流变性质会损害灌注,而当血细胞比容过低时,氧气输送会受到损害。这种情况下的最佳血红蛋白浓度尚未确定,异体红细胞输注的潜在不良影响是否会影响这一最佳血红蛋白浓度尚不清楚。合成红细胞具有优于内源性或输注红细胞的流变特性,具有增强灌注的潜力。迄今为止,对这一概念的探索仅限于动物模型,并取得了令人鼓舞的结果。经基因工程改造以表达血管平滑肌细胞增殖抑制剂的红细胞在冠状动脉移植物狭窄的动物模型中也取得了成功。在动物模型中,负载血红蛋白的脂质体已被用于缓解实体瘤中的缺氧效应,被认为是减少耐药性和转移的一种手段。一个明显的应用是在遗传性血红蛋白病的治疗中,但目前这仍处于实验阶段
合成血小板
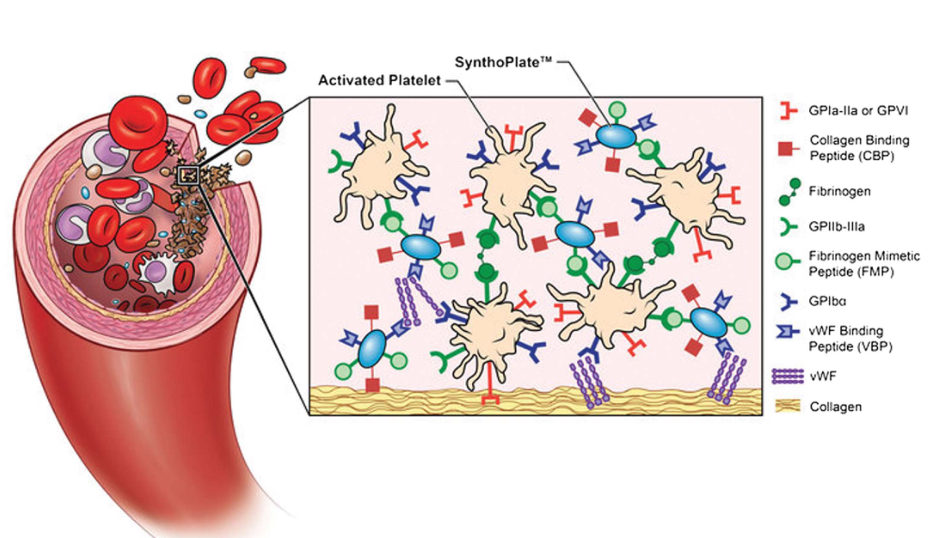
复制血小板至少部分功能的尝试包括纳米粒子技术和“血液制药”。纳米颗粒方法从相对简单的制剂到更复杂的胶囊不等,前者包括包封ADP的磷脂脂质体,并用代表纤维蛋白原γ链羧基末端序列的十二肽修饰,后者用多种受体肽序列修饰,并含有抗纤维蛋白溶解剂氨甲环酸。这两种方法目前都处于临床开发的不同阶段。ADP/纤维蛋白原序列脂质体正在日本进行临床试验,一种称为Synthoplate的纳米颗粒正在美国进行临床前开发。其他几个小组正在研究使用例如PLGA纳米球、白蛋白颗粒和修饰红细胞的纳米颗粒血小板替代物。迄今为止,这些努力仍处于开发的临床前阶段。
美国和其他地方的几个学术和工业实验室正在进行血小板的离体生产。血小板面临的一个特殊挑战是要求在生物反应器设计中包括一种在剪切下促进血小板通过膜脱落的方法。这个领域的一个著名代表是美国的血小板生物发生公司。它们产生由诱导多能干细胞分化成巨核细胞谱系的血小板。血小板的体外扩增在成本和工艺可扩展性方面面临着与红细胞生产相似的挑战,需要在临床试验中进行测试,以确定它们能够替代天然血小板的程度。
临床试验设计的挑战
评估合成血液产品的安全性和有效性的临床试验面临几个重大挑战。他们必须将新疗法与现有产品进行比较。在以前的开发工作中,有人认为像六溴环十二烷这样的“合成血液产品”可以与晶体或胶体相比较,因为标准血液产品在院前环境中是不可用的。在院前环境中提供标准血液产品的后勤挑战是巨大的,但是在许多创伤系统中,包括军事环境中,正在开发解决方案。因此,可能需要将新产品与标准血液产品进行比较的非劣效性试验设计,或者至少包括标准血液产品的复苏方法。此外,由于院前血液制品输血与死亡率降低有关,使用不太严格的终点,如血液制品利用率降低,可能不足以满足监管机构的要求。血液替代品临床开发的历史表明,新产品面临着一个充满挑战的监管环境和一个需要强大结果的临床机构。


